| Главная » Файлы » Физиология |
| [ Скачать с сервера (84.5 Kb) ] | 03.10.2009, 15:49 |
|
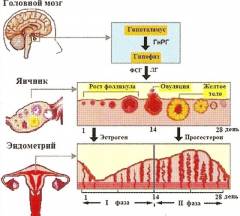
Первым (высшим) уровнем регуляции функционирования репродуктивной системы являются структуры, составляющие акцептор всех внешних и внутренних (со стороны подчиненных отделов) воздействий — кора головного мозга ЦНС и экстрагипоталамические церебральные структуры (лимбическая система, гиппокамп, миндалевидное тело). Адекватность восприятия ЦНС внешних воздействий и, как следствие, ее влияние на подчиненные отделы, регулирующие процессы в репродуктивной системе, зависят от характера внешних раздражителей (силы, частоты и длительности их действия), а также от исходного состояния ЦНС, влияющего на ее устойчивость к стрессовым нагрузкам. Хорошо известно о возможности прекращения менструаций при сильных стрессах (потеря близких людей, условия военного времени и т.д.), а также и без очевидных внешних воздействий при обшей психической неуравновешенности («ложная беременность» — задержка менструации при сильном желании или при сильной боязни забеременеть). Высшие регулирующие отделы репродуктивной системы воспринимают внутренние воздействия через специфические рецепторы к основным половым гормонам: эстрогенам, прогестерону и андро-генам. В ответ на внешние и внутренние стимулы в коре большого мозга и экстрагипоталамических структурах происходят синтез, выделение и метаболизм нейропептидов, неиротрансмиттеров, а также образование специфических рецепторов, которые в свою очередь избирательно влияют на синтез и выделение рилизинг-гормона гипоталамуса. К важнейшим нейротрансмиттерам, т.е. веществам-передатчикам, относятся норадреналин, дофамин, гамма-аминомасляная кислота (ГАМК), ацетилхолин, серотонин и мелатонин. Церебральные нейротрансмиттеры регулируют выработку гона-дотропин-рилизинг гормона (ГнРГ): норадреналин, ацетилхолин и ГАМК стимулируют их выброс, а дофамин и серотонин оказывают противоположное действие. Нейропептиды (эндогенные опиоидные пептиды — ЭОП, корти-котропин-рилизинг фактор и галанин) также влияют на функцию гипоталамуса и на сбалансированность функционирования всех звеньев репродуктивной системы. В настоящее время выделяют 3 группы ЭОП: энкефалины, эн-дорфины и динорфины. Эти субстанции обнаруживаются не только в различных структурах мозга и вегетативной нервной системы, но и в печени, легких, поджелудочной железе и других органах, а также в некоторых биологических жидкостях (плазма крови, содержимое фолликула). По современным представлениям, ЭОП вовлечены в регуляцию образования ГнРГ. Повышение уровня ЭОП подавляет секрецию ГнРГ, а следовательно, и выделение ЛГ и ФСГ, что, возможно, является причиной ановуляции, а в более тяжелых случаях — аменореи. Именно с повышением ЭОП связывают возникновение различных форм аменореи центрального генеза при стрессе, а также при чрезмерных физических нагрузках, например у спортсменок. Назначение ингибиторов опиоидных рецепторов (препаратов типа налоксона) нормализует образование ГнРГ, что способствует нормализации овуляторной функции и других процессов в репродуктивной системе у больных с аменореей центрального генеза. При снижении уровня половых стероидов (при возрастном или хирургическом выключении функции яичников) ЭОП не оказывает ингибирующего действия на высвобождение ГнРГ, что, вероятно, становится причиной усиленной продукции гонадотропинов у женщин в постменопаузе. Таким образом, сбалансированность синтеза и последующих метаболических превращений нейротрансмиттеров, нейропептидов и нейромодуляторов в нейронах мозга и в надгипоталамических структурах обеспечивает нормальное течение процессов, связанных с овуляторной и менструальной функцией. Вторым уровнем регуляции репродуктивной функции является гипоталамус, в частности его гипофизотропная зона, состоящая из нейронов вентро- и дорсомедиальных аркуатных ядер, которые обладают нейросекреторной активностью. Эти клетки имеют свойства как нейронов (воспроизводящих регулирующие электрические импульсы), так и эндокринных клеток, которые оказывают либо стимулирующее (либерины), либо блокирующее (статины) действие. Активность нейросекреции в гипоталамусе регулируется как половыми гормонами, которые поступают из кровотока, так и нейро-трансмиттерами и нейропептидами, образуемыми в коре головного мозга и надгипоталамических структурах. Гипоталамус секретирует ГнРГ, содержащие фолликулостиму-лирующий (РГФСГ — фоллиберин) и лютеинизирующий (РГЛГ — люлиберин) гормоны, которые воздействуют на гипофиз. Рилизинг-гормон ЛГ (РГЛГ — люлиберин) выделен, синтезирован и подробно описан. Выделить и синтезировать рилизинг-фол-ликулостимулирующий гормон до настоящего времени не удалось. Однако установлено, что декапептид РГЛГ и его синтетические аналоги стимулируют выделение гонадотрофами не только Л Г, но и ФСГ. В связи с этим принят один термин для гонадотропных либеринов — гонадотропин-рилизинг гормон (ГнРГ), по сути являющийся синонимом РГЛГ. Не был также идентифицирован и ги-поталамический либерин, стимулирующий образование пролакти-на, хотя установлено, что его синтез активируется ТТГ-рилизинг гормоном (тиролиберином). Образование пролактина активируется также серотонином и стимулирующими серотонинергические системы эндогенными опиоидными пептидами. Дофамин, наоборот, тормозит освобождение пролактина из лактотрофов аденогипофиза. Применение дофаминэргических препаратов типа парлодела (бромкриптина) позволяет успешно лечить функциональную и органическую гиперпролактинемию, являющуюся весьма распространенной причиной нарушений менструальной и овуляторной функций. Секреция ГнРГ генетически запрограммирована и носит пульсирующий (цирхоральныи) характер: пики усиленной секреции гормона продолжительностью несколько минут сменяются 1—3-часовыми интервалами относительно низкой секреторной активности. Частоту и амплитуду секреции ГнРГ регулирует уровень эстрадиола — выбросы ГнРГ в преовуляторный период на фоне максимального выделения эстрадиола оказываются значительно больше, чем в раннюю фолликулярную и лютеиновую фазы. Третьим уровнем регуляции репродуктивной функции является передняя доля гипофиза, в которой секретируются гонадотропные гормоны — фолликулостимулирующий, или фоллитропин (ФСГ), и лютеинизирующий, или лютропин (Л Г), пролактин, адренокорти-котропный гормон (АКТГ), соматотропный гормон (СТГ) и тирео-тропный гормон (ТТГ). Нормальное функционирование репродуктивной системы возможно лишь при сбалансированном выделении каждого из них. ФСГ стимулирует в яичнике рост и созревание фолликулов, пролиферацию гранулезных клеток; образование рецепторов ФСГ и ЛГ на гранулезных клетках; активность ароматаз в зреющем фолликуле (это усиливает конверсию андрогенов в эстрогены); продукцию ингибина, активина и инсулиноподобных факторов роста. Л Г способствует образованию андрогенов в тека-клетках; овуляции (совместно с ФСГ); ремоделированию гранулезных клеток в процессе лютеинизации; синтезу прогестерона в желтом теле. Пролактин оказывает многообразное действие на организм женщины. Его основная биологическая роль — стимуляция роста молочных желез, регуляция лактации, а также контроль секреции прогестерона желтым телом путем активации образования в нем рецепторов к ЛГ. Во время беременности и лактации прекращается ингибиция синтеза пролактина и, как следствие, возрастание его уровня в крови. К четвертому уровню регуляции репродуктивной функции относятся периферические эндокринные органы (яичники, надпочечники, щитовидная железа). Основная роль принадлежит яичникам, а другие железы выполняют собственные специфические функции, одновременно поддерживая нормальное функционирование репродуктивной системы. В яичниках происходят рост и созревание фолликулов, овуляция, образование желтого тела, синтез половых стероидов.
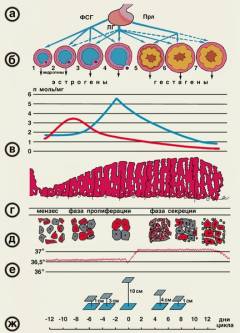
Фолликулогенез начинается под влиянием ФСГ в позднюю часть лютеиновой фазы цикла и заканчивается в начале пика выделения гонадотропинов. Примерно за I день до начала менструации снова повышается уровень ФСГ, что обеспечивает вступление в рост фолликулов (1—4-й день цикла), селекцию фолликула из когорты однородных — квазисинхронизированных (5—7-й день), созревание доминантного фолликула (8-12-й день) и овуляцию (13-15-й день). Этот процесс, который составляет фолликулярную фазу, длится около 14 дней. В результате формируется пре-овуляторный фолликул, а остальные из когорты вступивших в рост фолликулов подвергаются атрезии. Селекция единственного фолликула, предназначенного к овуляции, неотделима от синтеза в нем эстрогенов. Устойчивость продукции эстрогенов зависит от взаимодействия тека и гранулезных клеток, активность которых, в свою очередь, модулируется многочисленными эндокринными, паракринными и аутокринными механизмами, регулирующими рост и созревание фолликулов. В зависимости от стадии развития и морфологических признаков выделяют примордиальные, преантральные, антральные и пре-овуляторные, или доминантные, фолликулы. Примордиальный фолликул состоит из незрелой яйцеклетки, которая расположена в фолликулярном и гранулезном (зернистом) эпителии. Снаружи фолликул окружен соединительнотканной оболочкой (тека-клетки). В течение каждого менструального цикла от 3 до 30 примордиальных фолликулов начинают расти, преобразуясь в преантральные (первичные) фолликулы. Преантральный фолликул. В преантральном фолликуле овоцит увеличивается в размере и окружается мембраной, называемой блестящей оболочкой. Клетки гранулезного эпителия пролиферируют и округляются, образуя зернистый слой фолликула, а слой теки образуется из окружающей стромы. Для этой стадии характерна активация продукции эстрогенов, образуемых в гранулезном слое. Преовуляторный (доминантный) фолликул выделяется среди растущих фолликулов наиболее крупным размером (диаметр к моменту овуляции достигает 20 мм). Доминантный фолликул имеет богато васкуляризированный слой тека-клеток и гранулезных клеток с большим количеством рецепторов к ФСГ и ЛГ. Наряду с ростом и развитием доминантного преовуляторного фолликула в яичниках параллельно происходит атрезия остальных первоначально вступивших в рост (рекрутированных) фолликулов, а также продолжается атрезия примордиальных фолликулов. За время созревания в преовуляторном фолликуле происходит 100-кратное увеличение объема фолликулярной жидкости. В процессе созревания антральных фолликулов состав фолликулярной жидкости изменяется. Антралъный (вторичный) фолликул претерпевает увеличение полости, образуемой накапливающейся фолликулярной жидкостью, продуцируемой клетками гранулезного слоя. Активность образования половых стероидов при этом также возрастает. В тека-клетках синтезируются андрогены (андростендион и тестостерон). Попадая в клетки гранулезы, андрогены активно подвергаются ароматизации, обусловливающей их конверсию в эстрогены. На всех стадиях развития фолликула, кроме преовуляторного, содержание прогестерона находится на постоянном и относительно низком уровне. Гонадотропинов и пролактина в фолликулярной жидкости всегда меньше, чем в плазме крови, причем уровень пролактина имеет тенденцию к снижению по мере созревания фолликула. ФСГ определяется с начала формирования полости, а ЛГ можно выявить только в зрелом преовуляторном фолликуле вместе с прогестероном. Фолликулярная жидкость содержит также окситоцин и вазопрессин. Основным источником эстрогенов (эстрадиола, эстрио-ла и эстрона), из которых наиболее активен эстрадиол, является яичник. Кроме эстрогенов, в яичниках продуцируются прогестерон и определенное количество андрогенов. Помимо стероидных гормонов и ингибинов, поступающих в кровоток и оказывающих воздействие на органы-мишени, В яичниках синтезируются и биологически активные соединения с преимущественно локальным гормоноподобным действием. Так, образуемые простагландины, окситоцин и вазопрессин играют важную роль в качестве 1риггеров овуляции. Окситоцин оказывает и лютеолитическое действие, обеспечивая регресс желтого тела. Релаксин способствует овуляции и оказывает токолитическое действие на миометрий. Ростовые факторы — эпидермальный фактор роста (ЭФР) и инсулиноподобные факторы роста 1 и 2 (ИПФР-1 и ИПФР-2) активируют пролиферацию клеток гранулезы и созревание фолликулов. Эти же факторы участвуют совместно с гонадотропинами в тонкой регуляции процессов селекции доминантного фолликула, атрезии дегенерирующих фолликулов всех стадий, а также в прекращении функционирования желтого тела. Образование андрогенов в яичниках остается стабильным на протяжении всего цикла. Основное биологическое предназначение циклической секреции половых стероидов в яичнике состоит в регуляции физиологических циклических изменений эндометрия. Овуляция — разрыв преовуляторного (доминантного) фолликула и выход из него яйцеклетки. Овуляция сопровождается кровотечением из разрушенных капилляров, окружающих тека-клетки. Полагают, что овуляция происходит через 24—36 ч после преовуляторного пика эстрадиола, вызывающего резкий подъем секреции ЛГ. На этом фоне активизируются протеститические ферменты — коллагеназа и плазмин, разрушающие коллаген стенки фолликула и таким образом уменьшающие ее прочность. Одновременно отмечаемое повышение концентрации простагландина F, а также окситоцина индуцирует разрыв фолликула в результате стимуляции ими сокращения гладких мышц и выталкивания ооцита с яйценосным холмиком из полости фолликула. Разрыву фолликула способствует также повышение в нем концентрации простагландина Е2 и релаксина, уменьшающих ригидность его стенок. После выхода яйцеклетки в полость овулировавшего фолликула быспро врастают образующиеся капилляры. Гранулезные клетки подвергаются лютеинизации, морфологически проявляющейся в увеличении их объема и образовании липидных включений. Данный процесс, приводящий к образованию желтого тела, стимулируется ЛГ, активно взаимодействующим со специфическими рецепторами гранулезных клеток. Желтое тело - транзиторное гормонально-активное образование, функционирующее в течение 14 дней независимо от обшей продолжительности менструального цикла. Если беременность не наступила, желтое тело регрессирует. Полноценное желтое тело развивается только в фазе, когда в преовуляторном фолликуле образуется адекватное количество гранулезных клеток с высоким содержанием рецепторов ЛГ.
Гормоны яичников не только определяют функциональные изменения в самой репродуктивной системе. Они также активно влияют на обменные процессы в других органах и тканях, имеющих рецепторы к половым стероидам. Эти рецепторы могут быть как цитоплазменными (цитозоль-рецепторы), так и ядерными. Цито-плазменные рецепторы строго специфичны к эстрогенам, прогестерону и тестостерону, а ядерные могут быть акцепторами не только стероидных гормонов, но и аминопептидов, инсулина и глюкагона. Для прогестерона по рецепторному связыванию антагонистами считаются глюкокортикоиды. В коже под влиянием эстрадиола и тестостерона активируется синтез коллагена, что способствует поддержанию ее эластичности. Повышенная сальность, акне, фолликулиты, пористость и избыточное оволосение ассоциируются с усилением воздействия андрогенов. В костях эстрогены, прогестерон и андрогены поддерживают нормальное ремоделирование, предупреждая костную резорбцию. В жировой ткани баланс эстрогенов и андрогенов предопределяет как активность ее метаболизма, так и распределение в организме. Половые стероиды (прогестерон) заметно модулируют работу гипоталамического центра терморегуляции. С рецепторами к половым стероидам в ЦНС, в структурах гип-покампа, регулирующих эмоциональную сферу, а также в центрах, контролирующих вегетативные функции, связывают феномен «менструальной волны» в дни, предшествующие менструации. Данный феномен проявляется разбалансировкой процессов активации и торможения в коре, колебаниями тонуса симпатической и парасимпатической систем (особенно заметно влияющих на функционирование сердечно-сосудистой системы), а также изменением настроения и некоторой раздражительностью. У здоровых женщин эти изменения, однако, не выходят за физиологические границы. Пятый уровень регуляции репродуктивной функции составляют чувствительные к колебаниям уровней половых стероидов внутренние и внешние отделы репродуктивной системы (матка, маточные трубы, слизистая влагалища), а также молочные железы. Наиболее выраженные циклические изменения происходят в эндометрии. Циклические изменения в эндометрии касаются поверхностного слоя, состоящего из компактных эпителиальных клеток, и промежуточного, которые отторгаются во время менструации. Базальный слой, не отторгаемый во время менструации, обеспечивает восстановление десквамированных слоев. течения (менструация). Фаза пролиферации (фолликулярная) продолжается в среднем 12—14 дней, начиная с 5-го дня цикла. В этот пеРиод образуется новый поверхностный слой с вытянутыми трубчатыми железами, выстланными цилиндрическим эпителием с повышенной митотической активностью. Толщина функционального слоя эндометрия составляет 8 мм. Фаза секреции (лютеиновая) связана с активностью желтого тела, длится 14 дней. В этот период эпителий желез эндометрия начинает вырабатывать секрет, содержащий кислые ЛИКОЗамИЛОГЛИКанЫ, ГЛИКОПротеиды Активность секреции становится наивысшей на 20—21-й день. К этому времени в эндометрии обнаруживается максимальное количество протеолитических ферментов, а в строме происходят децидуальные превращения (клетки компактного слоя укрупняются, приобретая округлую или полигональную форму, в их цитоплазме накапливается гликоген). Отмечается резкая васкуляризация стромы — спиральные артерии резко извиты, образуют «клубки», обнаруживаемые во всем функциональном слое. Вены расширены. Такие изменения в эндометрии, отмечаемые на 20—22-й день (6—8-й день после овуляции) 28-дневного менструального цикла, обеспечивают наилучшие условия для имплантации оплодотворенной яйцеклетки. К 24-27-му дню в связи с началом регресса желтого тела и снижением концентрации продуцируемых им гормонов трофика эндометрия нарушается с постепенным нарастанием в нем дегенеративных изменений. Из зернистых клеток стромы эндометрия выделяются гранулы, содержащие релаксин, подготавливающий менструальное отторжение слизистой оболочки. В поверхностных участках компактного слоя отмечаются лаку парные расширения капилляров и кровоизлияния в строму, что можно обнаружить за I сут до начала менструации. Менструация включает десквамацию и регенерацию функционального слоя эндометрия. В связи с регрессом желтого тела и резким снижением содержания половых стероидов в эндометрии нарастает гипоксия. Началу менструации способствует длительный спазм артерий, приводящий к стазу крови и образованию тромбов. Гипоксию тканей (тканевой ацидоз) усугубляют повышенная проницаемость эндотелия, ломкость стенок сосудов, многочисленные мелкие кровоизлияния и массивная лейкоцитарная инфильтрация. Выделяемые из лейкоцитов лизосомальные протеолитические ферменты усиливают расплавление тканевых элементов. Вслед за дли тельным спазмом сосудов наступает их паретическое расширение с усиленным притоком крови. При этом отмечаются рост гидростатического давления в микроциркуляторном русле и разрыв стенок сосудов, которые к этому времени в значительной степени утрачивают свою механическую прочность. На этом фоне и происходит активная десквамация некротизированных участков функционального слоя. К концу 1-х суток менструации отторгается 2/3 функционального слоя, а полная его десквамация обычно заканчивается на 3-й день. Регенерация эндометрия начинается сразу же после отторжения некротизированного функционального слоя. Основой для регенерации являются эпителиальные клетки стромы базального слоя. В физиологических условиях уже на 4-й день цикла вся раневая поверхность слизистой оболочки оказывается эпителизированной. Далее опять следуют циклические изменения эндометрия — фазы пролиферации и секреции. Последовательные изменения на протяжении цикла в эндометрии: пролиферация, секреция и менструация зависят не только от циклических колебаний уровней половых стероидов в крови, но и от состояния тканевых рецепторов к этим гормонам. Концентрация ядерных рецепторов эстрадиола увеличивается до середины цикла, достигая пика к позднему периоду фазы пролиферации эндометрия. После овуляции наступает быстрое снижение концентрации ядерных рецепторов эстрадиола, продолжающееся до поздней секреторной фазы, когда их экспрессия становится значительно ниже, чем в начале цикла. Установлено, что индукция образования рецепторов как к эстрадиолу, так и к прогестерону зависит от концентрации в тканях эстрадиола. В раннюю пролиферативную фазу содержание рецепторов к прогестерону ниже, чем к эстрадиолу, но затем наступает предовуляторный подъем уровня рецепторов к прогестерону. После овуляции уровень ядерных рецепторов к прогестерону достигает максимума за весь цикл. В пролиферативной фазе происходит прямая стимуляция эстрадиолом образования рецепторов к прогестерону, что объясняет отсутствие связи между уровнем прогестерона в плазме и содержанием его рецепторов в эндометрии. Регуляция местной концентрации эстрадиола и прогестерона опосредована в большой степени появлением различных ферментов в течение менструального цикла. Содержание эстрогенов в эндометрии зависит не только от их уровня в крови, но и от образования. Эндометрий женщины способен синтезировать эстрогены путем превращения андростендиона и тестостерона с участием аро-матазы (ароматизация). Этот локальный источник эстрогенов усиливает эстрогенизацию клеток эндометрия, характеризующую про-лиферативную фазу. Во время этой фазы отмечаются самая высокая способность к ароматизации андрогенов и самая низкая активность ферментов, метаболизирующих эстрогены. В последнее время установлено, что эндометрий способен сек-ретировать и пролактин, полностью идентичный гипофизарному. Синтез пролактина эндометрием начинается во второй половине лютеиновой фазы (активируется прогестероном) и совпадает с де-цидуализацией стромальных клеток. Цикличность деятельности репродуктивной системы определяется принципами прямой и обратной связи, которая обеспечивается специфическими рецепторами гормонам в каждом из звеньев. Прямая связь состоит в стимулирующем действии гипоталамуса на гипофиз и в последующем образовании половых стероидов в яичнике. Обратная связь определяется влиянием повышенной концентрации половых стероидов на вышележащие уровни. Во взаимодействии звеньев репродуктивной системы различают «длинную», «короткую» и «ультракороткую» петли. «Длинная» петля — воздействие через рецепторы гипоталамо-гипофизарной системы на выработку половых гормонов. «Короткая» петля определяет связь между гипофизом и гипоталамусом. «Ультракороткая» петля — связь между гипоталамусом и нервными клетками, которые осуществляют локальную регуляцию с помощью нейротрансмиттеров, ней-ропептидов, нейромодуляторов и электрическими стимулами. Похожие статьи | |
| Просмотров: 25980 | Загрузок: 773 | Рейтинг: 4.0/4 | |
| Всего комментариев: 0 | |